Brennstoffzellen: Wie sie funktionieren und was sie bringen
Das Bordkraftwerk gewinnt elektrische Energie aus Wasserstoff

"Houston, wir haben ein Problem": Der klassische Hilferuf aus dem Jahr 1970 stand in engem Zusammenhang mit der Brennstoffzelle, die bei Apollo 13 als Energiequelle diente. Damals führte ein Kurzschluss zur Explosion eines Sauerstofftanks. Die Brennstoffzellen versagten, und so hatte das Hauptmodul des Raumfahrzeugs keinen Strom mehr. Folge: Die Besatzung musste fast sechs Tage im ungeheizten Mondlandemodul ausharren. Das Ganze ging glimpflich aus: Die geplante Mondlandung wurde gestrichen, aber die Besatzung kehrte heil zur Erde zurück.
Schon 1838 erfunden
Der Apollo-13-Unfall war wohl das spektakulärste Ereignis in der langen Geschichte der Brennstoffzelle, die Christian Friedrich Schönbein schon 1838 erfand. Heute wird seine Erfindung zum Beispiel in U-Booten und Stadtbussen genutzt, aber auch schon in Pkw-Prototypen. Wir erklären, wie die Technik funktioniert.
Protonenaustausch durch die Membran
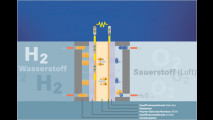
In der gängigsten Brennstoffzelle werden Wasserstoff und Sauerstoff zu Wasser umgewandelt. Die gewonnene elektrische Energie wird dann vom Elektromotor in Vortrieb umgesetzt. Der Wasserstoff stammt meist aus Gastanks, der Sauerstoff aus der Luft. Außerdem braucht man noch die Brennstoffzelle selbst. Die oft verwendete Variante mit Protonenaustausch-Membran (Proton Exchange Membrane Fuel Cell, PEMFC) besteht im Wesentlichen aus zwei Elektroden und einer Kunststoffmembran dazwischen. Letztere kann zum Beispiel aus Nafion bestehen, einer modifizierten Form von Teflon. Das Material hat die Eigenschaft, dass es positiv geladene Ionen (Kationen) leitet. In der Brennstoffzelle lässt die Membran Wasserstoffionen passieren, also Protonen.
Verschiedene Wanderwege
Die Membran ist auf beiden Seiten mit Elektrodenmaterial beschichtet – meist Kohlenstoff Kohlenstoff mit einem Edelmetall-Katalysator wie Platin. Auf der einen Seite, der Anode, wird Wasserstoff aufgespaltet in die positiven Wasserstoffi onen und negativ geladene Elektronen (Bild oben links). Beide wandern zur anderen Elektrode, der Kathode. Aber sie nehmen verschiedene Wege: Die Protonen wandern wie erwähnt durch die Membran, die Elektronen bewegen sich durch eine elektrische Leitung. An der Kathode angekommen, wandeln die Elektronen Sauerstoff in zweifach negativ geladene Oxid- Ionen um. Diese werden mit den Protonen, die aus der Membran kommen, zu Wasser (Bild oben rechts). Im Endeff ekt haben Wasserstoff und Sauerstoff zu Wasser reagiert. Dabei sind Elektronen gefl ossen, es wurde also ein Strom erzeugt. Da eine einzelne Zelle weniger als ein Volt liefert, werden oft hunderte Zellen hintereinandergeschaltet – zum so genannten Stack.
Hoch- oder Niedrigtemperatur
Bei der geschilderten Brennstoffzelle handelt es sich um eine Niedrigtemperatur-Brennstoffzelle. Solche Zellen werden bei ,nur" etwa 80 Grad Celsius betrieben. Sie werden unter anderem in der Mercedes B-Klasse F-Cell, im Opel/GM HydroGen 4 oder im Honda FCX eingesetzt. Zu den Nachteilen gehört die aufwendige Kühlung des Stacks. Eine Alternative ist die von VW favorisierte Hochtemperatur-Brennstoff zelle, die bei etwa 120 Grad arbeitet.
Vor- und Nachteile
Zu den Vorteilen von Brennstoffzellen-Fahrzeugen gehört der im Vergleich zum Verbrennungsmotor deutlich höhere Wirkungsgrad. Ein Nachteil ist die geringe Energiedichte: Bei 200 bar zum Beispiel enthält gasförmiger Wasserstoff nur etwa ein Fünftel der Energie von Erdgas. Weitere Probleme sind die fehlenden Wasserstoff-Tankstellen und die derzeit praktizierte Herstellung von Wasserstoff aus Erdgas – denn dabei entsteht wie im Verbrennungsmotor klimaschädliches CO2.
Einige 100.000 Stück bis 2015?
Noch sind bei der Brennstoffzelle zahlreiche Probleme zu lösen. VW betrachtet den angestrebten Serienstart im Jahr 2020 als nicht sicher. Dagegen gaben Mercedes, Ford, General Motors, Honda, Hyundai, Kia, Renault, Nissan und Toyota kürzlich gemeinsam bekannt, dass sie bis 2015 eine nennenswerte Zahl von Brennstoffzellen-Autos auf den Markt bringen wollen. Die Rede ist von einigen hunderttausend Stück weltweit.
Schon 1838 erfunden
Der Apollo-13-Unfall war wohl das spektakulärste Ereignis in der langen Geschichte der Brennstoffzelle, die Christian Friedrich Schönbein schon 1838 erfand. Heute wird seine Erfindung zum Beispiel in U-Booten und Stadtbussen genutzt, aber auch schon in Pkw-Prototypen. Wir erklären, wie die Technik funktioniert.
Protonenaustausch durch die Membran
In der gängigsten Brennstoffzelle werden Wasserstoff und Sauerstoff zu Wasser umgewandelt. Die gewonnene elektrische Energie wird dann vom Elektromotor in Vortrieb umgesetzt. Der Wasserstoff stammt meist aus Gastanks, der Sauerstoff aus der Luft. Außerdem braucht man noch die Brennstoffzelle selbst. Die oft verwendete Variante mit Protonenaustausch-Membran (Proton Exchange Membrane Fuel Cell, PEMFC) besteht im Wesentlichen aus zwei Elektroden und einer Kunststoffmembran dazwischen. Letztere kann zum Beispiel aus Nafion bestehen, einer modifizierten Form von Teflon. Das Material hat die Eigenschaft, dass es positiv geladene Ionen (Kationen) leitet. In der Brennstoffzelle lässt die Membran Wasserstoffionen passieren, also Protonen.
Verschiedene Wanderwege
Die Membran ist auf beiden Seiten mit Elektrodenmaterial beschichtet – meist Kohlenstoff Kohlenstoff mit einem Edelmetall-Katalysator wie Platin. Auf der einen Seite, der Anode, wird Wasserstoff aufgespaltet in die positiven Wasserstoffi onen und negativ geladene Elektronen (Bild oben links). Beide wandern zur anderen Elektrode, der Kathode. Aber sie nehmen verschiedene Wege: Die Protonen wandern wie erwähnt durch die Membran, die Elektronen bewegen sich durch eine elektrische Leitung. An der Kathode angekommen, wandeln die Elektronen Sauerstoff in zweifach negativ geladene Oxid- Ionen um. Diese werden mit den Protonen, die aus der Membran kommen, zu Wasser (Bild oben rechts). Im Endeff ekt haben Wasserstoff und Sauerstoff zu Wasser reagiert. Dabei sind Elektronen gefl ossen, es wurde also ein Strom erzeugt. Da eine einzelne Zelle weniger als ein Volt liefert, werden oft hunderte Zellen hintereinandergeschaltet – zum so genannten Stack.
Hoch- oder Niedrigtemperatur
Bei der geschilderten Brennstoffzelle handelt es sich um eine Niedrigtemperatur-Brennstoffzelle. Solche Zellen werden bei ,nur" etwa 80 Grad Celsius betrieben. Sie werden unter anderem in der Mercedes B-Klasse F-Cell, im Opel/GM HydroGen 4 oder im Honda FCX eingesetzt. Zu den Nachteilen gehört die aufwendige Kühlung des Stacks. Eine Alternative ist die von VW favorisierte Hochtemperatur-Brennstoff zelle, die bei etwa 120 Grad arbeitet.
Vor- und Nachteile
Zu den Vorteilen von Brennstoffzellen-Fahrzeugen gehört der im Vergleich zum Verbrennungsmotor deutlich höhere Wirkungsgrad. Ein Nachteil ist die geringe Energiedichte: Bei 200 bar zum Beispiel enthält gasförmiger Wasserstoff nur etwa ein Fünftel der Energie von Erdgas. Weitere Probleme sind die fehlenden Wasserstoff-Tankstellen und die derzeit praktizierte Herstellung von Wasserstoff aus Erdgas – denn dabei entsteht wie im Verbrennungsmotor klimaschädliches CO2.
Einige 100.000 Stück bis 2015?
Noch sind bei der Brennstoffzelle zahlreiche Probleme zu lösen. VW betrachtet den angestrebten Serienstart im Jahr 2020 als nicht sicher. Dagegen gaben Mercedes, Ford, General Motors, Honda, Hyundai, Kia, Renault, Nissan und Toyota kürzlich gemeinsam bekannt, dass sie bis 2015 eine nennenswerte Zahl von Brennstoffzellen-Autos auf den Markt bringen wollen. Die Rede ist von einigen hunderttausend Stück weltweit.
Bildergalerie: Brennstoffzellen-Technik
Auch interessant

Mercedes GLC vs. Audi Q5: deutsche Reise-SUVs im Daten-Vergleich

BMWs elektrischer M3 imitiert keinen V8. Er macht etwas Cooleres

Mercedes-AMG G 63 zu langweilig? Tuner Larte sorgt für Farbe

Tatsächlicher Verbrauch: Seat Ibiza 1,5 TSI (2026) im Test

Tatsächlicher Verbrauch: Mercedes CLA Mildhybrid (2026) im Test

Alle neuen Fiat-Modelle der näheren Zukunft im Überblick

Mercedes auf der Interschutz 2026: Lösungen von Arocs bis Zetros